哈医大二院吴健教授团队:Mettl14通过NF-κB/IL-6通路介导巨噬细胞炎症从而延缓动脉粥样硬化发生
2022年5月,哈尔滨医科大学附属二院吴健教授团队在Cellular and Molecular Life Sciences杂志上发表了题为“Mettl14 mediates the inflammatory response of macrophages in atherosclerosis through the NF-κB/IL-6 signaling pathway”的文章。
该研究发现了RNA m6A “writer”之一Mettl14可以调节动脉粥样硬化中巨噬细胞的炎症状态。具体而言,敲减Mettl14通过抑制Myd88 mRNA稳定性影响p65核转移以抑制IL-6表达,从而促进了巨噬细胞的M2极化并减少泡沫细胞的形成,延缓动脉粥样硬化的发展。这一发现为动脉粥样硬化的防治提供了新靶点和潜在的治疗策略。

首先,作者分析了冠心病患者外周血单核细胞PBMC中m6A修饰水平及相关酶学的变化,通过qRT-PCR证实冠心病患者PBMC的RNA甲基转移酶Mettl14的表达升高,并在腹腔注射LPS分离的巨噬细胞和LPS刺激的THP-1细胞中得到相同的结果。
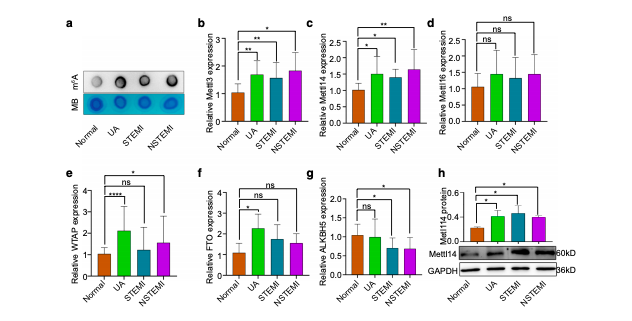
图1.冠心病患者中Mettl14表达升高
为了探索Mettl14在动脉粥样硬化中的作用,作者分别在siRNA敲减Mettl14的THP-1细胞和APOE-/-Mettl14-/+小鼠BMDM细胞中用流式细胞术及qRT-PCR验证M1和M2巨噬细胞的标志物表达情况,证实敲减Mettl14后能够促进巨噬细胞向M2型极化、抑制泡沫细胞形成及巨噬细胞迁移。
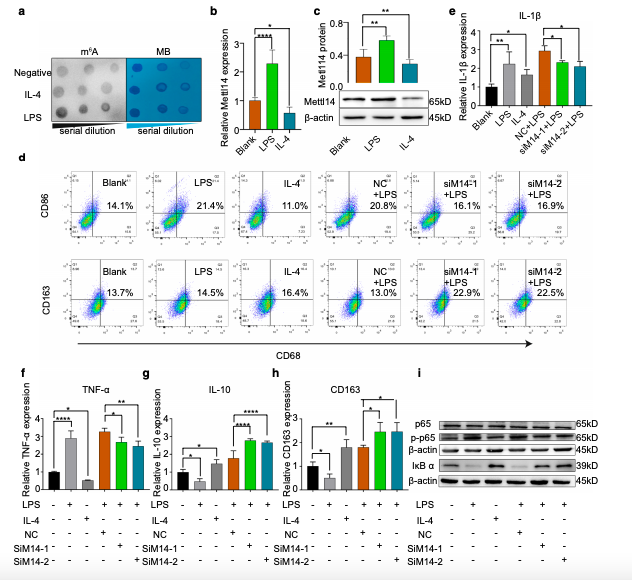
图2.敲除Mettl14能够促进巨噬细胞向M2型方向极化
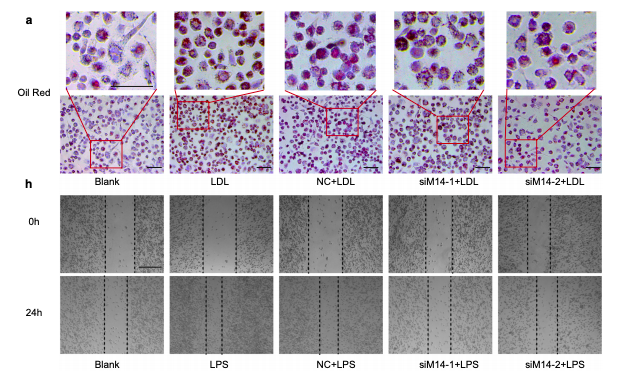
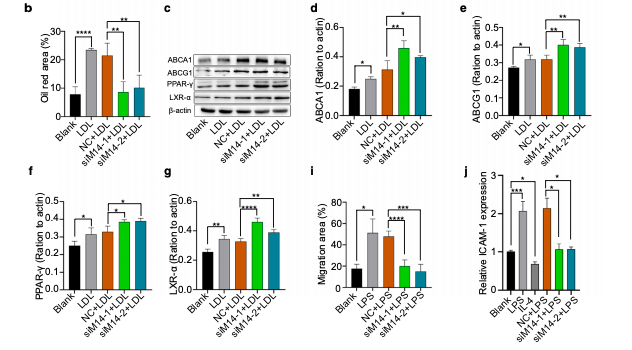
图3.敲除Mettl14能够抑制泡沫细胞形成、巨噬细胞迁移和粘附
通过转录组测序寻找Mettl14调控的靶基因,GO和KEGG分析显示差异基因主要参与免疫反应、炎症反应等,进一步证实了Mettl14调控巨噬细胞炎症反应。差异基因中与NF-κB通路关系密切的Myd88和IL-6引起了研究者的关注。虽然Mettl14均能促进Myd88和IL-6的表达,但是Mettl14影响Myd88的稳定性,对IL-6却无相同作用。进一步RIP实验证实了Mettl14对Myd88的直接调控作用。免疫荧光、核质分离蛋白印迹提示Mettl14促进p65的核转位,ChIP实验显示敲减Mettl14后p65与IL-6启动子结合减少,过表达Myd88可逆转上述现象。因此,Mettl14通过Myd88/NF-κB途径调节IL-6表达。
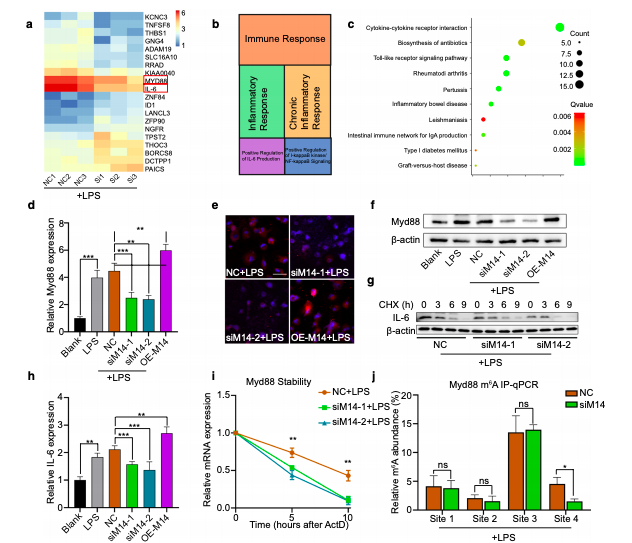
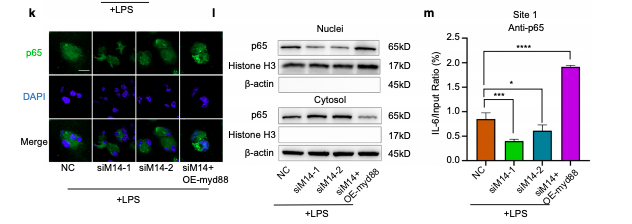
图4. Mettl14通过Myd88/NF-κB通路调控IL-6表达
为了验证Mettl14通过Myd88调控巨噬细胞功能,研究者在THP-1细胞中共同转染Mettl14过表达载体和针对Myd88的siRNA以实现营救实验的目的。结果显示,Mettl14调控巨噬细胞的功能均被siMyd88逆转,包括炎症因子的表达、泡沫细胞的形成和迁移功能。
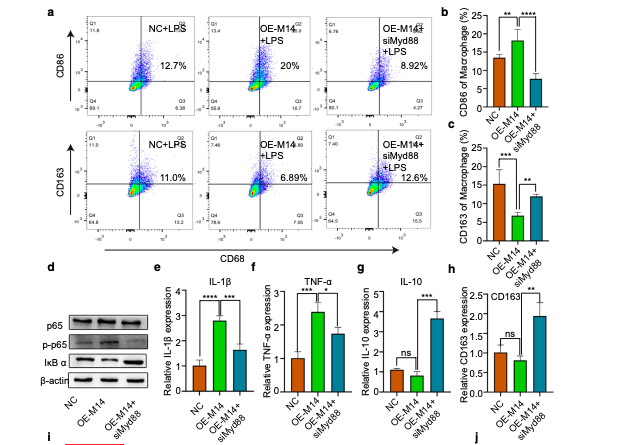
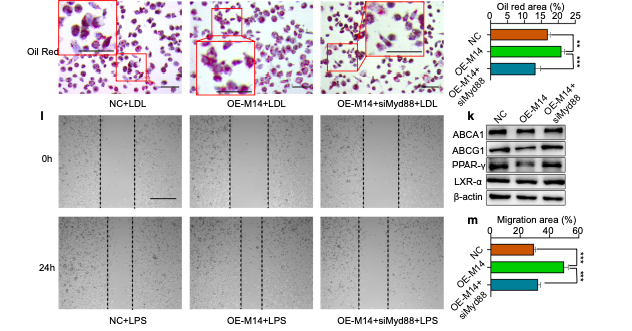
图5. Mettl14通过Myd88调控巨噬细胞炎症反应
最后,为了进一步验证Mettl14对动脉粥样硬化的作用,研究者对APOE-/-和APOE-/-Mettl14-/+小鼠高脂饮食诱导动脉粥样硬化斑块,主动脉弓图像及主动脉根部染色显示Mettl14敲减降低斑块和坏死区域面积,增加胶原蛋白含量、纤维帽厚度以及斑块稳定性。流式细胞术结果显示APOE-/-Mettl14-/+小鼠外周血单核细胞以Ly6ClowCX3CR1high为主,免疫荧光结果显示小鼠斑块内M2标记物CD206水平升高,M1标记物CD86和Myd88水平下降,ELISA结果显示小鼠血浆中IL-6水平降低。
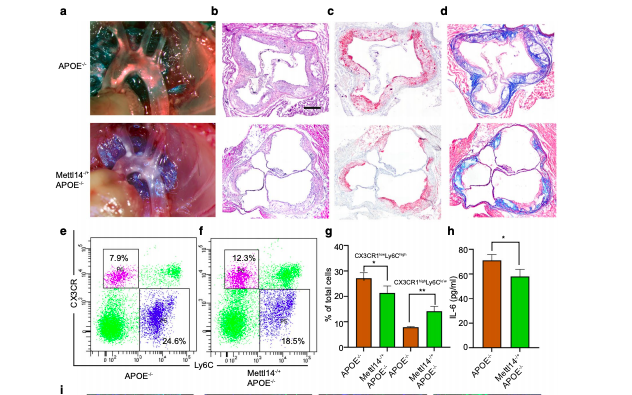
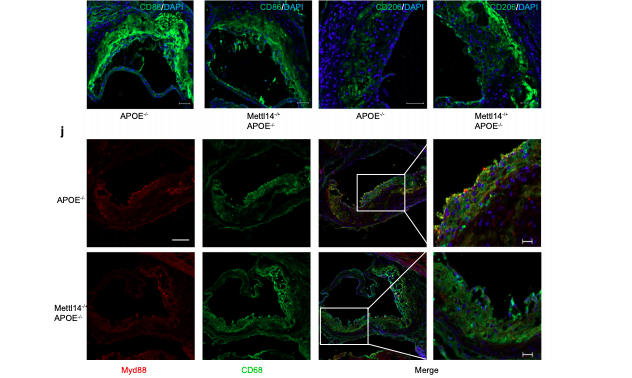
图6.体内证实Mettl14通过Myd88抑制动脉粥样硬化进展
综上,本研究从新的表观遗传学角度探讨了巨噬细胞炎症的调控机制,证实敲减Mettl14通过m6A修饰降低Myd88 mRNA的稳定性,从而增加M2巨噬细胞极化并减少泡沫细胞形成,同时还证明Mettl14通过Myd88/NF-κB途径调节IL-6表达,最终发挥抗动脉粥样硬化的作用。该发现提示巨噬细胞Mettl14可能是治疗和预防动脉粥样硬化的新靶点。
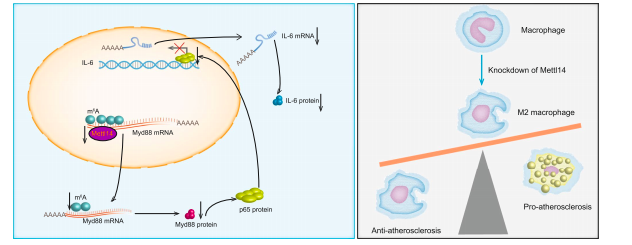
图7.本研究机制图
哈尔滨医科大学附属第二医院心内科吴健教授、孙勇教授为该论文的通讯作者,博士研究生郑阳为该论文的第一作者。
原文链接:https://link.springer.com/article/10.1007/s00018-022-04331-0